Lý thuyết Hóa 12: Bài 27. Nhôm và hợp chất của nhôm | Myphamthucuc.vn
Nội dung bài viết
Lý thuyết Hóa 12 Bài 27. Nhôm và hợp chất của nhôm
A. Nhôm
I. Vị trí trong bảng tuần hoàn, cấu hình electron nguyên tử
Nhôm (Al) ở ô số 13, thuộc nhóm IIIA, chu kì 3 của bảng tuần hoàn.
Cấu hình electron nguyên tử: 1s22s22p63s23p1; viết gọn là [Ne]3s23p1.
Nhôm dễ nhường cả 3 electron hóa trị nên có số oxi hóa +3 trong các hợp chất.
II. Tính chất vật lí
Nhôm là kim loại màu trắng bạc, nóng chảy ở 660oC, khá mềm, dễ kéo sợi, dễ dát mỏng. Có thể dát được những lá nhôm mỏng 0,01 mm dùng làm giấy gói kẹo, gói thuốc lá,…
Nhôm là kim loại nhẹ (D = 2,7 g/cm3), dẫn điện tốt (gấp 3 lần sắt, bằng 2/3 lần đồng) và dẫn nhiệt tốt (gấp 3 lần sắt).
III. Tính chất hóa học
Nhôm là kim loại có tính khử mạnh, chỉ sau kim loại kiềm và kiềm thổ, nên dễ bị oxi hóa thành ion dương.
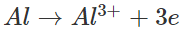
1. Tác dụng với phi kim
Nhôm khử dễ dàng các nguyên tử phi kim thành ion âm.
– Tác dụng với halogen:
Bột nhôm tự bốc cháy khi tiếp xúc với khí clo.
– Tác dụng với oxi
Khi đốt, bột nhôm cháy trong không khí với ngọn lửa sáng chói, tỏa nhiều nhiệt.
Nhôm bền trong không khí ở nhiệt độ thường do có màng oxit Al2O3 rất mỏng và bền bảo vệ.
2. Tác dụng với axit
– Nhôm khử dễ dàng ion H+ trong dung dịch HCl và H2SO4 loãng thành khí H2.
– Nhôm tác dụng mạnh với dung dịch HNO3 loãng, HNO3 đặc, nóng và H2SO4 đặc, nóng. Trong các phản ứng này, Al khử
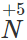
hoặc
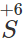
xuống số oxi hóa thấp hơn.
– Nhôm bị thụ động bởi dung dịch axit HNO3 đặc, nguội hoặc H2SO4 đặc, nguội nên có thể dùng thùng nhôm để chuyên chở những axit đặc, nguội này.
3. Tác dụng với oxit kim loại
Ở nhiệt độ cao, Al khử được nhiều ion kim loại trong oxit.
Thí dụ phản ứng giữa bột nhôm và sắt oxit gọi là phản ứng nhiệt nhôm. Nhiệt lượng do phản ứng tỏa ra lớn làm sắt nóng chảy nên phản ứng này được dùng để điều chế một lượng nhỏ sắt nóng chảy khi hàn đường ray.
4. Tác dụng với nuớc
Nếu phá bỏ lớp oxit trên bề mặt nhôm (hoặc tạo thành hỗn hống Al – Hg), thì nhôm sẽ tác dụng với nước ở nhiệt độ thường.
Nhôm không tác dụng với nước, dù ở nhiệt độ cao là vì trên bề mặt của nhôm được phủ kín một lớp Al2O3 rất mỏng, bền và mịn, không cho nước và khí thấm qua.
5. Tác dụng với dung dịch kiềm
Al2O3 là oxit lưỡng tính nên lớp màng mỏng Al2O3 trên bề mặt nhôm tác dụng với dung dịch kiềm tạo ra muối tan. Khi không còn màng oxit bảo vệ, nhôm sẽ tác dụng với nước tạo ra Al(OH)3 và giải phóng khí H2; Al(OH)3 là hiđroxit lưỡng tính nên tác dụng tiếp với dung dịch kiềm.
Như vậy, nhôm có thể tan trong dung dịch kiềm và giải phóng khí hiđro.
IV. Ứng dụng và trạng thái tự nhiên
1. Ứng dụng
– Nhôm và hợp kim của nhôm có ưu điểm là nhẹ, bền đối với không khí và nước nên được dùng làm vật liệu chế tạo máy bay, ô tô, tên lửa, tàu vũ trụ.
– Nhôm và hợp kim của nhôm có màu trắng bạc, đẹp nên được dùng trong xây dựng nhà cửa và trang trí nội thất.
– Nhôm nhẹ, dẫn điện tốt nên được dùng làm dây dẫn điện thay cho đồng. Do dẫn nhiệt tốt, ít bị gỉ và không độc nên nhôm được dùng làm dụng cụ nhà bếp.
– Bột nhôm trộn với bột sắt oxit (gọi là hỗn hợp tecmit) để thực hiện phản ứng nhiệt nhôm dùng hàn đường ray.
2. Trạng thái tự nhiên
Nhôm là kim loại hoạt động mạnh nên trong tự nhiên chỉ tồn tại ở dạng hợp chất. Nhôm là nguyên tố đứng hàng thứ ba sau oxi và silic về độ phổ biến trong vỏ Trái Đất. Hợp chất của nhôm có mặt khắp nơi, như có trong đất sét (Al2O3.2SiO2.2H2O), mica (K2O.Al2O3.6SiO2), boxit (Al2O3.2H2O), criolit (3NaRAlF3),…
V. Sản xuất nhôm
Trong công nghiệp, nhôm được sản xuất bằng phương pháp điện phân nhôm oxit nóng chảy.
1. Nguyên liệu
Nguyên liệu là quặng boxit Al2O3.2H2O. Boxit thường lẫn tạp chất là Fe2O3 và SiO2. Sau khi loại bỏ tạp chất bằng phương pháp hóa học thu được Al2O3 gần nguyên chất.
2. Điện phân nhôm oxit nóng chảy
Nhiệt độ nóng chảy của Al2O3 rất cao (2050oC), vì vậy phải hòa tan Al2O3 trong criolit nóng chảy để hạ nhiệt độ nóng chảy của hỗn hợp xuống 900oC.
– Quá trình điện phân:
Cực âm (catot) của thùng điện phân là một tấm than chì nguyên chất được bố trí ở đáy thùng. Ở catot xảy ra quá trình khử ion Al3+ thành Al.
Nhôm nóng chảy được định kì tháo ra từ đáy thùng.
Cực dương (anot) cũng là những khối than chì lớn. Ở anot xảy ra quá trình oxi hoá ion O2- thành khí O2.
Khí O2 ở nhiệt độ cao đốt cháy C thành khí CO và CO2. Vì vậy, sau một thời gian phải thay thế điện cực dương.
B. Một số hợp chất quan trọng của nhôm
I. Nhôm oxit
1. Tính chất
Nhôm oxit (Al2O3) là chất rắn, màu trắng, không tan trong nước và không tác dụng với nước, nóng chảy ở trên 2050oC.
Nhôm oxit là oxit lưỡng tính, vừa tác dụng với axit, vừa tác dụng với bazơ.
2. Ứng dụng
Trong tự nhiên, nhôm oxit tồn tại dưới dạng ngậm nước và dạng khan.
– Dạng oxit ngậm nước là thành phần chủ yếu của quặng boxit (Al2O3.2H2O) dùng để sản xuất nhôm.
– Dạng oxit khan, có cấu tạo tinh thể là đá quý ít phổ biến, thường gặp là:
+ Corinđon ở dạng tinh thể trong suốt, không màu, rất rắn, được dùng để chế tạo đá mài, giấy nhám,…
+ Trong tinh thể Al2O3, nếu một số ion Al3+ được thay bằng ion Cr3+ ta có hồng ngọc dùng làm đồ trang sức, chân kính đồng hồ và dùng trong kĩ thuật laze.
+ Tinh thể Al2O3 có lẫn tạp chất Fe2+, Fe3+ và Ti4+ ta có saphia dùng làm đồ trang sức.
+ Bột nhôm oxit dùng trong công nghiệp sản xuất chất xúc tác cho tổng hợp hữu cơ.
II. Nhôm hiđroxit
Nhôm hiđroxit (Al(OH)3) là chất rắn, màu trắng, kết tủa ở dạng keo.
Al(OH)3 là hiđroxit lưỡng tính.
Nhôm hiđroxit thể hiện tính bazơ trội hơn tính axit. Do có tính axit nên nhôm hiđroxit còn có tên là axit aluminic. Axit aluminic là axit rất yếu, yếu hơn axit cacbonic.
III. Nhôm sunfat
Muối nhôm sunfat khan tan trong nước tỏa nhiệt làm dung dịch nóng lên do bị hiđrat hóa.
Muối nhôm sunfat có nhiều ứng dụng nhất là muối sunfat kép của nhôm và kali ngậm nước gọi là phèn chua, công thức: K2SO4.Al2(SO4)3. 24H2O, hay viết gọn là: KAl(SO4)2.2H2O. Phèn chua được dùng trong ngành thuộc da, công nghiệp giấy, chất cầm màu trong ngành nhuộm vải, chất làm trong nước,…
Trong công thức hóa học trên, nếu thay ion K+ bằng Li+, Na+ hay NH4+ ta được các muối kép khác có tên chung là phèn nhôm (nhưng không gọi là phèn chua).
IV. Cách nhận biết ion Al3+ trong dung dịch
Cho từ từ dung dịch NaOH đến dư vào dung dịch thí nghiệm, nếu thấy có kết tủa keo xuất hiện rồi tan trong NaOH dư thì chứng tỏ có ion Al3+.
Xem thêm Giải Hóa 12: Bài 27. Nhôm và hợp chất của nhôm