Sơ đồ tư duy Hóa 10 chương 4 | Myphamthucuc.vn
Hệ thống lý thuyết Hóa 10 qua Sơ đồ tư duy Hóa 12 chương 4 chi tiết, đầy đủ nhất. Tổng hợp loạt bài hướng dẫn lập Sơ đồ tư duy Hóa 10 hay, ngắn gọn
A. Sơ đồ tư duy Hóa 10 chương 4: Phản ứng Oxi hóa khử
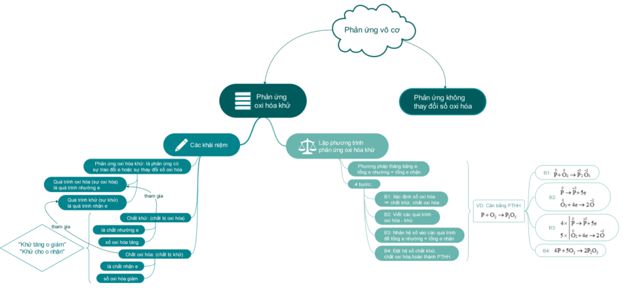
B. Lý thuyết hóa 10 chương 4 ngắn nhất
PHẢN ỨNG ÔXI HÓA KHỬ là phản ứng trong đó nguyên tử (hay ion) này nhường electron cho nguyên tử (hay ion) kia.
Trong một phản ứng oxi hoá – khử thì quá trình oxi hoá và quá trình khử luôn luôn xảy ra đồng thời.
Điều kiện phản ứng ôxi hóa – khử là chất ôxi hóa mạnh tác dụng với chất khử mạnh để tạo thành chất oxi hóa và chất khử yếu hơn.
1. CHẤT ÔXI HÓA là chất nhận electron, kết quả là số oxi hóa giảm.
Nếu hợp chất có nguyên tử (hay ion) mang soh cao nhất là chất ôxi hóa (SOH cao nhất ứng với STT nhóm) hay soh trung gian (sẽ là chất khử nếu gặp chất oxi hóa mạnh).
Ion kim loại có soh cao nhất Fe3+, Cu2+, Ag+…
ANION NO3– trong môi trường axit là chất ôxi hóa mạnh (sản phẩm tạo thành là NO2, NO, N2O, N2, hay NH4); trong môi trường kiềm tạo sản phẩm là NH3 (thường tác dụng với kim loại mà oxit và hiđrôxit là chất lưỡng tính); trong môi trường trung tính thì xem như không là chất oxi hóa.
H2SO4 ĐẶC là chất oxi hóa mạnh (tạo SO2, S hay H2S)
MnO4– còn gọi là thuốc tím (KMnO4) trong môi trường H+ tạo Mn2+(không màu hay hồng nhạt), môi trường trung tính tạo MnO2 (kết tủa đen), môi trường OH– tạo MnO42- (xanh).
HALOGEN
ÔZÔN
2. CHẤT KHỬ là chất nhường electron, kết quả là số oxi hóa tăng.
Nếu hợp chất có nguyên tử (hay ion) mang soh thấp nhất là chất khử (soh thấp nhất ứng với 8 – STT nhóm) hay chứa số oxi hoá trung gian (có thể là chất oxi hóa khi gặp chất khử mạnh)
Đơn chất kim loại, đơn chất phi kim (C, S, P, N…).
Hợp chất (muối, bazơ, axit, oxit) như: FeCl2, CuS2, Fe(OH)3, HBr, H2S, CO, Cu2O…
Ion (cation, anion) như: Fe2+, Cl–, SO32-…
3. QUÁ TRÌNH OXI HÓA là quá trình (sự) nhường electron.
4. QUÁ TRÌNH KHỬ là quá trình (sự) nhận electron.
5. SỐ OXI HOÁ là điện tích của nguyên tử (điện tích hình thức) trong phân tử nếu giả định rằng các cặp electron chung coi như chuyển hẳn về phía nguyên tử có độ âm điện lớn hơn.
Qui ước 1: Số oxi hoá của nguyên tử dạng đơn chất bằng không
Fe Al H2 O2 Cl2
Qui ước 2: Trong phân tử hợp chất, số oxi hoá của nguyên tử Kim loại nhóm A là +n; Phi kim nhóm A trong hợp chất với kim loại hoặc hyđro là 8 – n (n là STT nhóm)
-
Kim loại hoá trị 1 là +1: Ag+1Cl Na2+1SO4 K+1NO3
-
Kim loại hoá trị 2 là +2: Mg+2Cl2 Ca+2CO3 Fe+2SO4
-
Kim loại hoá trị 3 là +3: Al+3Cl3 Fe2+3(SO4)3
-
Của oxi thường là –2: H2O-2 CO2-2 H2SO4-2 KNO3-2
-
Riêng H2O2-1 F2O+2
-
Của Hidro thường là +1: H+1Cl H+1NO3 H2+1S
Qui ước 3: Trong một phân tử tổng số oxi hoá của các nguyên tử bằng không.
H2SO4 2(+1) + x + 4(-2) = 0 → x = +6
K2Cr2O7 2(+1) + 2x + 7(-2) = 0 → x = +6
Qui ước 4: Với ion mang điện tích thì tổng số oxi hoá của các nguyên tử bằng điện tích ion. Mg2+ số oxi hoá Mg là +2, MnO4– số oxi hoá Mn là: x + 4(-2) = -1 → x = +7
6. CÂN BẰNG PHƯƠNG TRÌNH PHẢN ỨNG OXI HOÁ KHỬ:
B1. Xác định số oxi hoá các nguyên tố. Tìm ra nguyên tố có số oxi hoá thay đổi.
B2. Viết các quá trình làm thay đổi số oxi hoá
Chất có oxi hoá tăng: Chất khử – ne → số oxi hoá tăng
Chất có số oxi hoá giảm: Chất oxi hoá + me → số oxi hoá giảm
B3. Xác định hệ số cân bằng sao cho số e cho = số e nhận
B4. Đưa hệ số cân bằng vào phương trình, đúng chất và kiểm tra lại theo trật tự: kim loại – phi kim – hidro – oxi
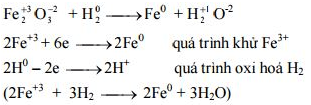
Cân bằng:
Fe2O3 + 3H2 → 2Fe + 3H2O
Chất oxi hoá chất khử
Fe3+ là chất oxi hoá H2 là chất khử
7. PHÂN LOẠI PHẢN ỨNG ÔXI HÓA KHỬ
Môi trường
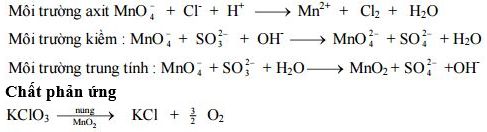
Phản ứng oxi hóa – khử nội phân tử: Là phản ứng oxi hóa – khử trong đó chất khử và chất oxi hóa đều thuộc cùng phân tử.
Phản ứng tự oxi hóa – tự khử là phản ứng oxi hóa – khử trong đó chất khử và chất oxi hóa đều thuộc cùng một nguyên tố hóa học, và đều cùng bị biến đổi từ một số oxi hóa ban đầu.
Cl2 + 2 NaOH → NaCl + NaClO + H2O
8. CÂN BẰNG ION – ELECTRON
– Phản ứng trong môi trường axit mạnh (có H+ tham gia phản ứng) thì vế nào thừa Oxi thì thêm H+ để tạo nước ở vế kia.
– Phản ứng trong môi trường kiềm mạnh (có OH– tham gia phản ứng) thì vế nào thừa Oxi thì thêm nước để tạo OH– ở vế kia.
– Phản ứng trong môi trường trung tính (có H2O tham gia phản ứng) nếu tạo H+, coi như H+ phản ứng; nếu tạo OH– coi như OH– phản ứng nghĩa là tuân theo các nguyên tắc đã nêu trên.
9. CẶP OXI HÓA – KHỬ là dạng oxi hóa và dạng khử của cùng một nguyên tố. Cu2+/Cu; H+/H2.
10. DÃY ĐIỆN HÓA là dãy những cặp oxi hóa – khử được xếp theo chiều tăng tính oxi hóa và chiều giảm tính khử.

11. CÁC CHÚ Ý ĐỂ LÀM BÀI TẬP
Khi hoàn thành chuỗi phản ứng tính số oxi hóa để biết đó là phản ứng oxi hóa – khử hay không.
Để chứng minh hoặc giải thích vai trò của một chất trong phản ứng thì trước hết dùng số oxi hóa để xác định vai trò và lựa chất phản ứng.
Toán nhớ áp dụng định luật bảo toàn electron dựa trên định luật bảo toàn nguyên tố theo sơ đồ.
Một chất có hai khả năng axit – bazơ mạnh và oxi hóa – khử mạnh thì xét đồng thời
Riêng một chất khi phản ứng với chất khác mà có cả 2 khả năng phản ứng axit – bazơ và oxi hoá – khử thì được xét đồng thời (thí dụ Fe3O4 + H+ + NO3–)
Hỗn hợp gồm Mn+, H+, NO3– thì xét vai trò oxi hóa như sau (H+, NO3–), H+, Mn+
C. Trắc nghiệm hóa 10 chương 4 đầy đủ đáp án
Câu 1: Số oxi hóa của lưu huỳnh (S) trong H2S, SO2, SO32-, SO42- lần lượt là
-
-2, +4, +4, +6
-
-2, +4, +6, +8
-
+2, +4, +8, +10
-
0, +4, +3, +8
Câu 2: Ở phản ứng nào sau đây NH3 đóng vai trò chất khử ?
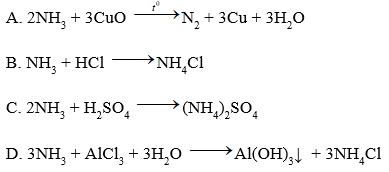
Câu 3: Trong phản ứng sau ![]() . Clo đóng vai trò là
. Clo đóng vai trò là
-
vừa là chất oxi hóa, vừa là chất khử
-
môt trường
-
chất khử
-
chất oxi hóa
Câu 4: Cho phản ứng hóa học: Fe + CuSO4 → FeSO4 + Cu. Trong phản ứng trên xảy ra
-
sự khử Fe2+và sự oxi hóa Cu.
-
sự khử Fe2+ và sự khử Cu2+.
-
sự oxi hóa Fe và sự oxi hóa Cu.
-
sự oxi hóa Fe và sự khử Cu2+.
Câu 5: Bạc tiếp xúc với không khí có H2S bị biến đổi thành Ag2S màu đen:
![]()
Câu nào diễn tả đúng tính chất của các chất phản ứng ?
-
H2S là chất khử, O2là chất oxi hóa
-
Ag là chất khử, O2là chất oxi hóa
-
H2S vừa là chất oxi hóa, vừa là chất khử, còn Ag là chất khử.
-
Ag là chất oxi hóa, H2S là chất khử
Câu 6: Cho biết các phản ứng xảy ra như sau
2FeBr2 + Br2 → 2FeBr3 (1) ;
2NaBr + Cl2 → 2NaCl + Br2 (2)
Phát biểu đúng là
-
Tính oxi hóa của clo mạnh hơn của Fe3+.
-
Tính oxi hóa của Br2 mạnh hơn của Cl2.
-
Tính khử của Br– mạnh hơn của Fe2+.
-
Tính khử của Cl– mạnh hơn của Br–.
Câu 7: Cho các phản ứng sau:
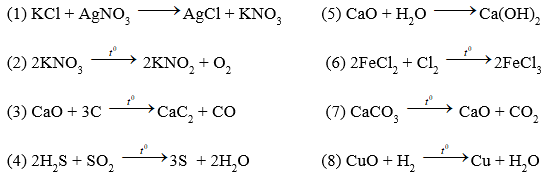
Nhóm gồm các phản ứng oxi hóa khử là
-
(2), (3), (4), (6), (8)
-
(2), (3), (4), (5), (6)
-
(2), (4), (6), (7), (8)
-
(1), (2), (3), (4), (5)
Câu 8: Trong phản ứng đốt cháy CuFeS2 tạo ra sản phẩm CuO, Fe2O3 và SO2 thì một phân tử CuFeS2 sẽ
-
nhận 13 electron.
-
nhận 12 electron.
-
nhường 13 electron.
-
nhường 12 electron.
Câu 9: Cho từng chất: Fe, FeO, Fe(OH)2, Fe(OH)3, Fe3O4, Fe2O3, Fe(NO3)2, Fe(NO3)3, FeSO4, Fe2(SO4)3, FeCO3 lần lượt phản ứng với HNO3 đặc, nóng. Số phản ứng thuộc loại phản ứng oxi hoá – khử là
-
8.
-
5.
-
7.
-
6.
Câu 10: Cho dãy các chất và ion: Zn, S, FeO, SO2, N2, HCl, Cu2+, Cl–. Số chất và ion có cả tính oxi hóa và tính khử là
-
7.
-
5.
-
4.
-
6.
Câu 11: Tổng hệ số (các số nguyên, tối giản) của tất cả các chất trong phương trình phản ứng giữa Cu với dung dịch HNO3 đặc, nóng là
-
10.
-
11.
-
8.
-
9.
Câu 12: Trong phản ứng: K2Cr2O7 + HCl → CrCl3 + Cl2 + KCl + H2O
Số phân tử HCl đóng vai trò chất khử bằng k lần tổng số phân tử HCl tham gia phản ứng. Giá trị của k là
-
4/7.
-
1/7.
-
3/14.
-
3/7.
Câu 13: Cho phương trình hoá học: Fe3O4 + HNO3 → Fe(NO3)3 + NxOy + H2O
Sau khi cân bằng phương trình hoá học trên với hệ số của các chất là những số nguyên, tối giản thì hệ số của HNO3 là
-
13x – 9y.
-
46x – 18y.
-
45x – 18y.
-
23x – 9y.
Câu 14: Cho phương trình phản ứng Al + HNO3 → Al(NO3)3 + N2O + N2 + H2O. Nếu tỉ lệ số mol N2O và N2 là 2:3 thì sau cân bằng ta có tỉ lệ mol Al : N2O : N2 là
-
23 : 4 : 6
-
46 : 2 : 3
-
20 : 2 : 3
-
46 : 6 : 9
Câu 15: Hòa tan hoàn toàn một lượng bột sắt vào dung dịch HNO3 loãng thu được hỗn hợp khí gồm 0,015 mol N2O và 0,01 mol NO. Lượng sắt đã hòa tan là
-
2,8g
-
1,4g
-
0,84g
-
0,56g
Câu 16: Cho phản ứng:
Na2SO3 + KMnO4 + NaHSO4 → Na2SO4 + MnSO4 + K2SO4 + H2O.
Tổng hệ số của các chất (là những số nguyên, tối giản) trong phương trình phản ứng là
-
47.
-
27.
-
31.
-
23.
Câu 17: Hòa tan hoàn toàn 19,2g Cu vào dung dịch HNO3 loãng, tất cả khí NO thu được đem oxi hóa thành NO2 rồi sục vào dòng nước có khí O2 để chuyển hết NO2 thành HNO3. Thể tích khí O2 (đktc) đã tham gia vào quá trình trên là:
-
4,48 lít
-
3,36 lít
-
2,24 lít
-
6,72 lít
Câu 18: Hòa tan hỗn hợp gồm 0,05 mol Ag và 0,03 mol Cu vào dung dịch HNO3 thu được hỗn hợp khí A gồm NO và NO2 có tỉ lệ mol tương ứng là 2:3 . Thể tích hỗn hợp khí A ở đktc là
-
3,3737 lít
-
1,369 lít
-
2,737 lít
-
2,224 lít
Câu 19: Nung nóng từng cặp chất trong bình kín: (1) Fe + S (r), (2) Fe2O3 + CO (k), (3) Au + O2 (k), (4) Cu + Cu(NO3)2 (r), (5) Cu + KNO3 (r) , (6) Al + NaCl (r). Các trường hợp xảy ra phản ứng oxi hoá kim loại là :
-
(1), (3), (6)
-
(2), (3), (4)
-
(1), (4), (5)
-
(2), (5), (6)
Câu 20: Hoà tan hoàn toàn 12,42 gam Al bằng dung dịch HNO3 loãng (dư), thu được dung dịch X và 1,344 lít (ở đktc) hỗn hợp khí Y gồm hai khí là N2O và N2. Tỉ khối của hỗn hợp khí Y so với khí H2 là 18. Cô cạn dung dịch X, thu được m gam chất rắn khan. Giá trị của m là
-
38,34.
-
34,08.
-
106,38.
-
97,98.
Câu 21: 1/ Có các phản ứng hoá học sau
-
CaCO3→ CaO + CO2
-
2KClO3 → 2KCl + 3O2
-
2NaNO3 → 2NaNO2 + O2
-
2Al(OH)3 → Al2O3 + 3H2O
-
2NaHCO3 → Na2CO3 + H2O + CO2
Phản ứng oxi hoá – khử là
-
(1), (4).
-
(2), (3).
-
(3), (4).
-
(4), (5).
Câu 22: Trong phản ứng:
2NO2 + 2NaOH → NaNO3 + NaNO2 + H2O
NO2 đóng vai trò
-
là chất oxi hoá.
-
là chất khử.
-
là chất oxi hoá, đồng thời cũng là chất khử.
-
không là chất oxi hoá, cũng không là chất khử.
Câu 23: Nhận định nào không đúng?
-
Trong các phản ứng hoá học, số oxi hoá của các nguyên tố có thể thay đổi hoặc không thay đổi.
-
Trong các phản ứng phân huỷ, số oxi hoá của các nguyên tố luôn thay đổi.
-
Trong các phản ứng thế, số oxi hoá của các nguyên tố luôn thay đổi.
-
Trong các phản ứng oxi hoá – khử luôn có sự thay đổi số oxi hoá của các nguyên tố.
Câu 24: Cho phương trình phản ứng hoá học sau:
4HClO3 + 3H2S → 4HCl + 3H2SO4
8Fe + 30 HNO3 → 8Fe(NO3)3 + 3N2O + 15H2O
16HCl + 2KMnO4 → 2KCl + 2MaCl2 + 8H2O + 5Cl2
Mg + CuSO4 → MgSO4 + Cu
2NH3 + 3Cl2 → N2 + 6HCl
Dãy các chất khử là
-
H2S, Fe, KMnO4, Mg, NH3.
-
H2S, Fe, HCl, Mg, NH3.
-
HClO3, Fe, HCl, Mg, Cl2.
-
H2S, HNO3, HCl, CuSO4, Cl2.
Câu 25: Trong các phản ứng sau, phản ứng tự oxi hoá – khử là
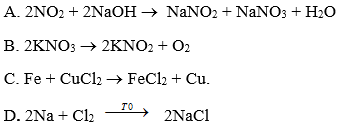
Câu 26: Trong các phản ứng sau, phản ứng nào HCl đóng vai trò là chất oxi hoá?
- 4HCl + MnO2 → MnCl2 + Cl2 + 2H2O
-
Zn + 2HCl → ZnCl2 + H2
-
HCl + NaOH → NaCl + H2O
-
2HCl + CuO → CuCl2 + H2O
Câu 27: Hãy sắp xếp các phân tử, ion cho dưới đây theo thứ tự tăng dần số oxi hoá của nitơ: NO2, NH3, NO–2, NO–3, N2, NO2.
-
NO2 < NO < NH3 < NO–2 < NO–3 < N2 < N2O.
-
NH3 < N2 < N2O < NO < NO–2 < NO2 < NO–3.
-
NH3 < N2 < NO < NO–2 < N2O < NO2 < NO–3.
-
NH3 < N2 < N2O < NO–2 < NH < N2 < NO–3.
Câu 28: Cho phương trình phản ứng:
4Zn + 5H2SO4 đặc/nóng
4ZnSO4 + X + 4H2O. X là
-
SO2 .
-
H2S.
-
S.
-
H2.
Câu 29: Cho sơ đồ phản ứng hoá học sau:
HNO3 + H2S → S + NO + H2O (1)
Cu + HNO3 → Cu(NO3)2 + H2O + NO (2)
Tổng hệ số (nguyên, tối giản) của các chất tham gia và tạo thành trong các phản ứng (1) và (2) lần lượt là
-
12 và 18.
-
14 và 20.
-
14 và 16.
-
12 và 20.
Câu 30: Trong các loại phản ứng sau, loại nào luôn là phản ứng oxi hoá khử?
-
Phản ứng hoá hợp.
-
Phản ứng phân huỷ.
-
Phản ứng trung hoà.
-
Phản ứng thế.
Câu 31: Cho sơ đồ phản ứng
FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + K2SO4 + MnSO4 + H2O
Hệ số cân bằng (nguyên, tối giản) của FeSO4 là
-
10.
-
8.
-
6.
-
2.
Câu 32: Lưu huỳnh tác dụng với dung dịch kiềm nóng theo phương trình sau
3S + 6KOH → 2K2S + K2SO3 + 3H2O
Trong phản ứng này có tỉ lệ số nguyên tử lưu huỳnh bị oxi hóa và số nguyên tử lưu huỳnh bị khử là
-
2:1.
-
1:2.
-
1:3.
-
2:3.
Câu 33: Lưu huỳnh tác dụng với axit sunfuric đặc nóng theo phương trình sau
S + 2H2SO4 → 3SO2 + 2H2O
Trong phản ứng này có tỉ lệ số nguyên tử lưu huỳnh bị khử và số nguyên tử lưu huỳnh bị oxi hóa là
-
1: 2.
-
1: 3.
-
3 :1.
-
2:1.
Câu 34: Cho sơ đồ phản ứng:
KMnO4 + H2O2 + H2SO4 → MnSO4 + O2 + K2SO4 + H2O
Hệ số (nguyên, tối giản) của chất oxi hóa, của chất khử là
-
3 và 5.
-
5 và 2.
-
2 và 5.
-
3 và 2.
Câu 35: Cho sơ đồ phản ứng:
H2SO4 + Fe → Fe2(SO4)3 + H2O + SO2
Số phân tử H2SO4 bị khử và số phân tử H2SO4 tạo muối của phản ứng sau khi cân bằng là
-
6 và 3.
-
3 và 6.
-
6 và 6.
-
3 và 3.
Câu 36: Tỷ lệ số phân tử HNO3 là chất oxi hóa và số phân tử HNO3 là môi trường trong phản ứng FeCO3 + HNO3 → Fe(NO3)3 + NO + CO2 + H2O là
-
8 : 1.
-
1 : 9.
-
1 : 8.
-
9 : 1.
Câu 37: Trong các ion (phân tử) cho dưới đây, ion (phân tử ) có tính oxi hóa là
-
Mg.
-
Cu2+.
-
Cl–.
-
S2-.
Câu 38: Cho sơ đồ phản ứng:
Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O
Số phân tử HNO3 bị khử và số phân tử tạo muối nitrat là
-
1 và 8.
-
10 và 5.
-
1 và 9.
-
8 và 2.
Câu 39: Cho sơ đồ phản ứng sau: FeS2 + HNO3 → Fe(NO3)3 + H2SO4 + NO2 + H2O
Tổng hệ số nguyên tối giản các chất tham gia phản ứng là
-
25.
-
44.
-
24.
-
19
Câu 40: Cho sơ đồ phản ứng sau FeS + HNO3 → Fe(NO3)3 + H2SO4 + NO + H2O
Trong phản ứng trên, khi phản ứng với 1 mol FeS có bao nhiêu mol axit đóng vai trò môi trường và bao nhiêu mol axit đóng vai trò chất oxi hoá?
-
2 mol HNO3 đóng vai trò môi trường, 4 mol HNO3 đóng vai trò chất oxi hoá.
-
4 mol HNO3 đóng vai trò môi trường, 2 mol HNO3 đóng vai trò chất oxi hoá.
-
3 mol HNO3 đóng vai trò môi trường, 3 mol HNO3 đóng vai trò chất oxi hoá.
-
1 mol HNO3 đóng vai trò môi trường, 5 mol HNO3 đóng vai trò chất oxi hoá.
Câu 41: Trong phản ứng : Fe + CuSO4 → FeSO4 + Cu , 1mol ion Cu2+ đã
-
nhường 1mol electron.
-
nhận 1mol electron.
-
nhận 2mol electron.
-
nhường 2mol electron.
Câu 42: Trong phản ứng 2NO2 + 2NaOH → NaNO3 + NaNO2 + H2O, khí NO2 là chất
-
chỉ bị oxi hoá.
-
chỉ bị khử.
-
không bị oxi hoá, không bị khử.
-
vừa bị oxi hoá, vừa bị khử.
Câu 43: Trong các phản ứng sau, ở phản ứng nào NH3 đóng vai trò chất oxi hóa?
-
2NH3+ 3Cl2 →N2+ 6HCl
-
2NH3+ 2Na → NaNH2 + H2
-
2NH3+ H2O2+ MnSO4 → MnO2 + ( NH4)2SO4
-
4NH3 + 5O2 → 4NO + 6 H2O
Câu 44: Trong các phản ứng dưới đây,phản ứng nào không phải là phản ứng oxi hoá-khử ?
-
Zn + 2HCl → ZnCl2 + H2
-
Mg + CuCl2 → MgCl2 + Cu
-
FeS + 2HCl → FeCl2 + H2S↑
-
Fe2(SO4)3 + Cu → 2FeSO4+ CuSO4
Câu 45: Cho sơ đồ phản ứng sau: M2Ox + HNO3 → M(NO3)3 + …..
Phản ứng trên thuộc loại phản ứng trao đổi khi x có giá trị là bao nhiêu?
-
x = 1.
-
x = 2.
-
x = 1 hoặc 2.
-
x = 3.
Câu 46: Nguyên tử Clo chuyển thành ion clorua bằng cách
-
nhận 1 electron
-
nhường 1 electron
-
nhận 1 proton
-
nhường1 proton
Câu 47: Nhận định nào không đúng?
-
Các phản ứng thế đều là phản ứng oxihoá khử.
-
Các phản ứng trao đổi có thể là phản ứng oxihoá khử, có thể không là phản ứng oxihoá khử.
-
Các phản ứng hoá hợp có thể là phản ứng oxihoá khử, có thể không là phản ứng oxihoá khử.
-
Các phản ứng trao đổi đều không phải là phản ứng oxihoá khử.
Câu 48: Nhóm các phần tử vừa có thể là chất khử, vừa có thể là chất oxihoá là
-
Cu , Fe2+.
-
Cu , Mg2+.
-
S+4 , Fe2+.
-
S+4, Cu
Câu 49: Sự biến đổi nào sau đây là sự khử?
-
2Cl– → Cl2 + 2.1e
-
Zn → Zn2+ + 2e
-
Mn+7 + 3e → Mn+4
-
Mn+7 → Mn+4 + 3e
Câu 50: Trong phản ứng 3Cu + 8HNO3 →” 3Cu(NO3)2 + 2NO + 4H2O
chất bị oxi hoá là
-
Cu.
-
Cu2+.
-
H+.
-
NO3-
Câu 51: Kim loại nào sau đây có tính khử mạnh nhất?
-
K.
-
Na.
-
Li.
-
Rb
Câu 52: Trong phản ứng của đồng với ion Fe3+ tạo ra ion Cu2+ và Fe2+ ta thấy
-
2 ion Fe3+ oxihoá 1 nguyên tử đồng.
-
1 ion Fe3+ oxihoá 1 nguyên tử đồng.
-
3 ion Fe3+ oxihoá 1 nguyên tử đồng.
-
2 ion Fe3+ khử 1 nguyên tử đồng.
Câu 53: Cho phương trình hoá học Fe + CuSO4 → FeSO4 + Cu
Trong quá trình phản ứng
-
khối lượng kim loại Fe tăng dần
-
khối lượng kim loại Cu giảm dần
-
nồng độ ion Cu2+ trong dung dịch tăng dần
-
nồng độ ion Fe2+ trong dung dịch tăng dần
Câu 54: Biến đổi nào sau đây phù hợp với sự bảo toàn điện tích?
-
Fe → Fe2+ + 3e
-
Fe3+ + 1e → Fe2+
-
Fe → Fe3+ + 2e
-
Fe2+ + 3e → Fe
Câu 55: Cho sơ đồ phản ứng : MnO2 + HCl → MnCl2 + Cl2 + H2O
Trong phản ứng trên, HCl có vai trò
-
chất oxihoá
-
chất khử
-
vừa là chất khử, vừa là môi trường
-
vừa là chất oxihoá, vừa là môi trường
Câu 56: Cho dòng khí CO dư qua ống đựng hỗn hợp bột các chất FeO, CuO thu được hỗn hợp rắn X. Hoà hỗn hợp X trong dung dịch HCl dư. Hỏi có bao nhiêu phản ứng oxihoá khử đã xảy ra trong quá trình trên?
-
4
-
3.
-
2.
-
1.
Câu 57: Chọn sản phẩm đúng cho sơ đồ phản ứng sau:
SO2 + KMnO4 + H2O → ………………
-
K2SO4 , MnSO4, H2O.
-
K2SO4 , MnO2, H2SO4.
-
KOH , MnSO4, H2SO4.
-
K2SO4 , MnSO4, H2SO4.
Câu 58: Trong môi trường axit H2SO4 ,chất nào làm mất màu dung dịch KMnO4 ?
-
CuCl2.
-
NaOH.
-
Fe2(SO4)3.
-
FeSO4.
Câu 59: Cho các quá trình sau:
(1) Đốt cháy than trong không khí .
(2) Làm bay hơi nước biển trong quá trình sản xuất muối.
(3) Nung vôi
(4) Tôi vôi .
(5) Iot thăng hoa.
Trong các quá trình trên, quá trình nào có phản ứng hóa học xảy ra là
-
(1), (2), (3), (4), (5).
-
(1), (2), (3).
-
(2), (3), (4), (5).
-
(1), (3), (4).
Câu 60: Nhận định nào không đúng?
-
Sự khử là sự mất electron.
-
Chất khử là chất nhường electron.
-
Chất oxi hóa là chất nhận electron.
-
Sự oxi hóa là sự mất electron.
Câu 61: Nhận định nào không đúng?
-
Phản ứng oxi hóa – khử là phản ứng luôn xảy ra đồng thời sự oxi hoá và sự khử
-
Phản ứng oxi hóa – khử là phản ứng trong đó có sự thay đổi số oxi hóa của một số nguyên tố.
-
Phản ứng oxi hóa – khử là phản ứng trong đó có sự thay đổi số oxi hóa của tất cả các nguyên tố.
-
Phản ứng oxi hóa – khử là phản ứng có sự chuyển electron giữa các chất phản ứng.
Câu 62: Cho quá trình sau: S+6 + 2e → S+4
Kết luận nào đúng?
-
Quá trình trên là quá trình oxi hóa .
-
Quá trình trên là quá trình khử.
-
Trong quá trình trên Sđóng vai trò là chất khử.
-
Trong quá trình trên Sđóng vai trò là chất oxi hóa.
Câu 63: Số oxi hóa của clo trong các trường hợp chất HCl, HClO, NaClO2, KClO3, HClO4 lần lượt là
-
-1, +1, +2, +3, +4.
-
-1, +1, +3, +5, +6.
-
-1, +1, +3, +5, +7.
-
-1, +1, +4, +5, +7.
Câu 64: Cho phản ứng: FeS + H2SO4 → Fe2(SO4)3 + SO4↑ + H2O
Hệ số cân bằng tối giản, nguyên của H2SO4 là
-
8
-
10 .
-
12.
-
4
Câu 65: Cho phản ứng sau:
Vai trò của NO2 là
-
chất oxi hóa.
-
Chất khử.
-
Vừa là chất oxi hóa, vừa là chất khử.
-
Không là chất oxi hóa, cũng không là chất khử.
|
Câu |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
ĐA |
A |
A |
A |
D |
B |
A |
A |
C |
C |
B |
|
Câu |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
ĐA |
A |
D |
B |
D |
A |
B |
B |
B |
C |
C |
|
Câu |
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
29 |
30 |
|
ĐA |
B |
C |
B |
B |
A |
B |
B |
B |
B |
D |
|
Câu |
31 |
32 |
33 |
34 |
35 |
36 |
37 |
38 |
39 |
40 |
|
ĐA |
A |
B |
D |
B |
D |
B |
B |
C |
D |
C |
|
Câu |
41 |
42 |
43 |
44 |
45 |
46 |
47 |
48 |
49 |
50 |
|
ĐA |
C |
D |
B |
C |
D |
A |
B |
C |
C |
A |
|
Câu |
51 |
52 |
53 |
54 |
55 |
56 |
57 |
58 |
59 |
60 |
|
ĐA |
D |
A |
D |
B |
C |
B |
D |
D |
D |
A |
|
Câu |
61 |
62 |
63 |
64 |
65 |
|||||
|
ĐA |
C |
B |
C |
B |
C |




















