Lý thuyết Hóa 8: Bài 42. Nồng độ dung dịch | Myphamthucuc.vn
Lý thuyết Hóa 8 Bài 42. Nồng độ dung dịch
1. NỒNG ĐỘ PHẦN TRĂM: (C%)
* Nồng độ phần trăm (kí hiệu C%) của dung dịch cho biết số gam chất tan có trong 100 gam dung dịch.
Công thức:
![]()
Trong đó : C% : nồng độ phần trăm của dung dịch (%)
mct : khối lượng chất tan (gam)
mdd : khối lượng dung dịch (gam) = mdung môi + mchất tan
Từ công thức tính nồng độ phần trăm, ta suy ra các công thức sau:
– Công thức tính khối lượng dung dịch:
![]()
– Công thức tính khối lượng chất tan:
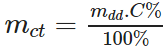
Ví dụ 1: Hoà tan 10 gam đường vào 40 gam nước. Tính nồng độ phần trăm của dung dịch thu được.
Giải:
Khối lượng chất tan là: mct = 10 gam
Khối lượng dung dịch thu được là: mdd = mdm + mct = 40 + 10 = 50 gam
Áp dụng công thức:
![]()
2. NỒNG ĐỘ MOL CỦA DUNG DỊCH (CM)
* Nồng độ mol (kí hiệu CM) của dung dịch cho biết số mol chất tan có trong một lít dung dịch.
Công thức tính: ![]()
Trong đó: CM là nồng độ mol (mol/lit)
n là số mol chất tan (mol)
Vdd là thể tích dung dịch (lit)
– Các công thức được suy ra từ công thức tính nồng độ mol của dung dịch:
+ Công thức tính số mol chất tan: n = CM . V
+ Công thức tính thể tích dung dịch:
![]()
Ví dụ: Tính khối lượng H2SO4 có trong 50 ml dung dịch H2SO4 2M
Giải:
Số mol H2SO4 có trong dung dịch H2SO4 2M là: nH2SO4 = CM . V = 2 . 0,05 = 0,1 mol
=> Khối lượng H2SO4 là: mH2SO4 = n . M = 0,1.98 = 9,8 gam
* Công thức chuyển đổi giữa nồng độ phần trăm và nồng độ mol:
Công thức tính nồng độ phần trăm:
![]()
Khối lượng dung dịch được tính theo công thức: mdd = Ddd . V
với Ddd là khối lượng riêng của dung dịch (gam/lít) ; V là thể tích của dung dịch (lít)
Khối lượng chất tan là: mct = n . M
Thay vào (1) ta có:
![]()
![]()
=> Công thức chuyển từ nồng độ phần trăm sang nồng độ mol:
![]()
Lưu ý: Công thức tính này lấy đơn vị của Ddd là gam/lít, thường các đầu bài cho đơn vị của Ddd là gam/ml nên ta cần đổi lại đơn vị để áp dụng công thức.
Xem thêm Giải Hóa 8: Bài 42. Nồng độ dung dịch






















